1、引言
多溴联苯是一系列含溴原子的芳香族化合物,具有高毒性、高沸点、半挥发性,在高温下热分解或燃烧时产生多溴二恶英。具有很强的脂溶性,不溶于水,在水中溶解度不超过30 (25℃)[1]
多溴联苯具有耐热和不易降解性能,被广泛使用于电子电器设备、自动控制设备、建筑材料和纺织品等商品化产品中。研究表明,多溴联苯具有类似的神经毒性,会对肝和神经系统的发育造成毒害,同时干扰甲状腺内分泌,可能致癌、引起生物性别错乱或免疫系统异常[2~5]。因此,越来越多国家开始关注起了多溴联苯物质的使用。
芬顿试剂用于氧化降解持久性有机物的报道不断出现。到目前作为废水的深度氧化法(AOP) 中的主流方法,芬顿试剂的应用范围正在不断扩展[6]。
芬顿降解的主要机理如下[7~9]:
H2O2 + Fe2+
→ OH· + OH− + Fe3+
或
Fe3+ + H2O2 →[FeIIIOOH]2+ + H+
无论哪一种机理,先后生成的OH·和OOH·都具有强氧化性,可以促进有机物的降解。使用Fenton法在处理一些难降解有机物(如苯酚类、苯胺类)方面显示出一定的优越性[10~16]。众多实验[17~22]结果显示,Fenton法氧化能力强、反应条件温和、设备也较为简单,适用范围比较广。但也存在处理费用高、工艺条件复杂、过程不易控制等缺点。
使用一般方法难以降解持久性有机污染物多溴联苯,只有芬顿试剂的强氧化能力才可以起到明显的作用。本文首次研究了H2O2/Fenton试剂法降解水中的4,4’-二溴联苯。该方法也适用于多溴联苯其余208种同族体的降解。
2、材料与方法
2.1实验材料
反应容器::100ml玻璃(自制);磁力搅拌器(含转子):85-1型,金坛市恒丰仪器厂;液相色谱:Agilent1100(美国安捷伦公司)
4,4’-二溴联苯(常州金坛化学有限公司),双氧水(国药集团化学试剂有限公司),无水乙醇(国药集团化学试剂有限公司),硫酸亚铁(广东汕头市西陇化工厂)均为分析醇,甲醇(上海陆都化学试剂厂)为色谱醇。
2.2实验方法
将4,4’-二溴联苯水溶液(乙醇为助溶剂)在自制容器中用磁力搅拌器搅拌一段时间,然后滴加一定量Fenton(H2O2/Fe2+)试剂,上用保鲜膜密封,循环水控温20℃左右,继续搅拌。反应每隔30min取样,样品采用美国安捷伦1100液相色谱仪分析。色谱柱为C18硅胶柱,与流动相甲醇构成反相色谱体系,控制温度35℃,检测波长:226nm;流速:1mL/min;进样量:20 ,具体分析方法参见SN T 2005.1-2005。实验装置见图2-1:
Fenton试剂法降解水中的4,4’-二溴联苯
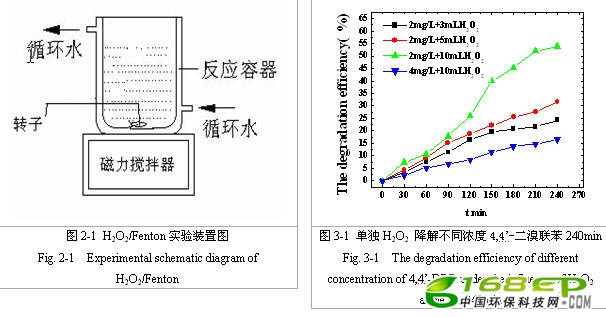
3、结果与讨论
3.1 单独过氧化氢降解实验
我们做了不同浓度不同投加量试验情况对比。分别滴加3mL、5mL和10mL30%过氧化氢于100 mL的2mg/L和4mg/L溶液中,充分搅拌240min,结果见图3-1。
由图3-1可知,过氧化氢单独降解2mg/L二溴联苯,随着过氧化氢的加入量的增加,降解率明显增加;在加入3mL、5mL和10mL30%过氧化氢反应240min后,降解率分别达到了24.4%,31.7%和53.9%,可见过氧化氢的强氧化性对于4,4’-DBB的降解起着一定作用。
实验同时也考察了4mg/L溶液的降解情况,结果表明,高浓度不利于降解。同样加入10mL
H2O2,240min后的降解率仅达16.5%,可见,H2O2对于低浓度的4,4’-DBB溶液降解效果较明显。
但是,考虑到加入过多过氧化氢时处理费用高,要实现彻底降解耗时较长,我们在以下实验中加入Fe2+,即研究芬顿试剂对4,4’-DBB降解率的影响。由于具有强氧化性自由基的生成,使得降解率在短时间内进一步提高。
3.2 芬顿试剂降解实验
根据文献[23],H2O2与亚铁离子的比例以及pH值对反应有很大影响。我们做了以下实验:
3.2.1不同H2O2/Fe2+摩尔比
降解浓度为2mg/L 的二溴联苯溶液100mL,结果见图3-2(1)。
由图3-2(1)可知,H2O2/Fe2+的摩尔比存在一个最佳值。分别取摩尔比为30:1,30:2,30:3,50:3,50:5,在摩尔比为30:3(即10:1)时,2mg/L溶液的降解率达最佳值。在过氧化氢加入量一定时,随着Fe2+浓度增加,降解率上升,当Fe2+超过一定值后,过量的Fe2+就会与溶液中生成的OH·反应,消耗掉一部分的自由基,从而减轻了氧化效果;同样,当Fe2+的量一定时,H2O2如果过量也会起到自由基清除的作用,因此,H2O2/Fe2+的恰当比例是获得最佳降解率的关键。
实验中也发现,当H2O2/Fe2+摩尔比为50:5(即10:1)时,降解率并没有因为投加量的增加而提高,相反降低了不少,分析原因是由于pH值得影响。摩尔比取30:1,30:2,30:3,50:3时,溶液pH值在2.0~2.4,而摩尔比为50:5时,pH值为1.4左右,由此可见溶液pH值对降解率影响较大。
Fenton试剂法降解水中的4,4’-二溴联苯
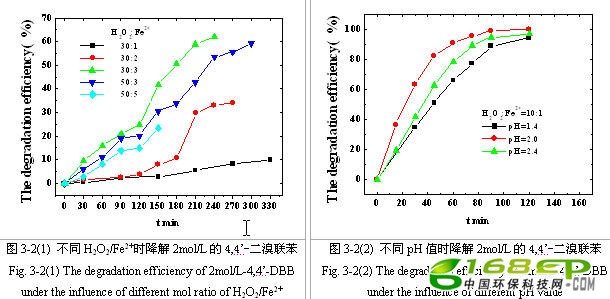
3.2.2 pH值影响
为了考察溶液pH值对降解率的影响,固定H2O2/Fe2+摩尔比为10:1,降解2mg/L 的二溴联苯溶液50mL,pH值分别取1.4,2.0,2.4,结果见图3-2(2)。
由图3-2(2)可知, pH值对二溴联苯降解起着重要作用,当H2O2/Fe2+固定时,存在最佳pH值。pH值在2左右时,降解达到最佳值;pH值在1.4左右是降解效果明显不如pH值在2附近时的效果;pH值在2.4左右时,效果也不如pH值为2时,而且随着反应过程中H+的消耗,溶液中逐渐呈现出絮凝状态。
我们还可以发现当芬顿试剂投加量比先前增加一倍后,降解率明显提高。在120min(即2h)内,在H2O2/Fe2+=10:1时,4,4’-DBB的降解率提高到99%以上,基本上实现了完全降解。
3.2.3不同初始浓度及投加量的影响
由于芬顿试剂对于降解低浓度4,4’-DBB取得了明显效果,我们进一步考察不同初始浓度对降解率的影响,以及在H2O2/Fe2+摩尔比一定(10:1)时,不同芬顿试剂投加量对降解率的影响。结果见图3-2(3)。
Fenton试剂法降解水中的4,4’-二溴联苯
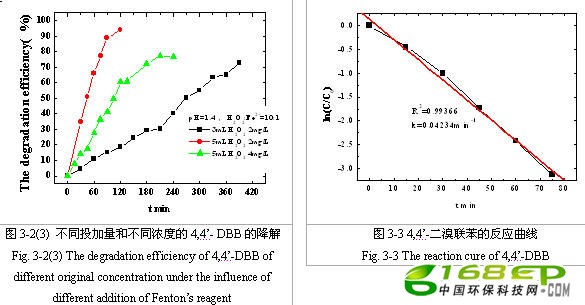
由图可知,在H2O2/Fe2+摩尔比,投加量一定时,低浓度的2mg/L溶液比较高浓度4mg/L溶液易于降解。在pH值在1.4左右时,可以看出明显差距:2mg/L的4,4’-DBB溶液投加5mL H2O2 (H2O2/Fe2+=10:1)后,120min内,降解率就达到94.3%,而同样的4mg/L的4,4’-DBB溶液,在240min后降解率才达到77%。
当H2O2投加量为3mL时,与投加量为5mL的相比,降解效果要差,390min后降解率才达到72.7%,由此可见芬顿试剂投加量也是决定降解的重要因素。
3.3 动力学研究
取H2O2/Fe2+摩尔比为10:1时,pH值为2左右,降解2mg/L的4,4’-DBB溶液2h。根据动力学反应原理,一级反应满足积分式:lnC=lnC0-kt,作lnC/C0~t关系曲线,结果见图3-3。
由图3-3可知,芬顿降解符合准一级反应规律,回归系数(R2)达到0.99366,其一级降解常数(k)为0.04234 min-1。
4.
结论
(1) 单独过氧化氢对于4,4’-DBB的降解有一定效果,反应时间越长降解效果越好;降解率随着过氧化氢加入量增加而增加;
(2) 芬顿试剂降解4,4’-DBB存在最佳H2O2/Fe2+摩尔比。本实验条件下,H2O2/Fe2+=10时效果最好;
(3) 芬顿试剂降解4,4’-DBB存在最佳pH值。实验证明,pH值在2左右时,降解效果最好;
(4) 芬顿试剂的投加量对于4,4’-DBB的降解起到重要作用。在摩尔比、pH值一定时,芬顿试剂加入量越多越利于加快降解;
(5) 低浓度4,4’-DBB溶液比较高浓度的溶液易于降解,且反应时间越长,降解率越好。
(6) 当H2O2和Fe2 +的摩尔比为10:1,pH =2时,处理初始浓度为2mg/ L 4,4’-DBB的水溶液2小时,4,4’-DBB去除率最高可达到99 %以上,说明芬顿试剂可将4,4’-DBB基本完全去除。
(7)
作lnC/C0~t关系曲线图,结果可以发现线性关系良好。可以推断4,4’-DBB的降解符合动力学一级反应。 |